परमाणु भौतिकी का परिचय (Introduction to Atomic Physics)
परमाणु ऊर्जा परमाणु रिएक्टरों और परमाणु हथियारों दोनों के लिए शक्ति का स्रोत है। यह ऊर्जा परमाणुओं के विभाजन (विखंडन) या जुड़ने (संलयन) से आती है। इस ऊर्जा के स्रोत को समझने के लिए, पहले परमाणु को समझना होगा।
एक परमाणु किसी तत्व का सबसे छोटा कण होता है जिसमें उस तत्व की विशेषता होती है। 1900 की शुरुआत तक परमाणु की प्रकृति के बारे में ज्ञान धीरे-धीरे बढ़ता गया। पहली सफलताओं में से एक 1911 में सर अर्नेस्ट रदरफोर्ड द्वारा हासिल की गई थी। उन्होंने स्थापित किया कि परमाणु का द्रव्यमान इसके नाभिक में केंद्रित है।


उन्होंने यह भी प्रस्तावित किया कि नाभिक का धनात्मक आवेश होता है और यह नकारात्मक रूप से आवेशित इलेक्ट्रॉनों से घिरा होता है, जिसकी खोज 1897 में जे जे थॉमसन ने की थी।
परमाणु संरचना का यह सिद्धांत 1913 में नील्स बोह्र द्वारा पूरक था। बोह्र परमाणु ने इलेक्ट्रॉनों को निश्चित गोले या क्वांटम स्तरों में रखा। परमाणु को समझना कई वैज्ञानिकों के लिए अभी भी एक फोकस बना हुआ है।
परमाणु की संरचना (Atomic Structure)
एक परमाणु एक सकारात्मक रूप से चार्ज किए गए नाभिक के बारे में परिभाषित गोले में व्यवस्थित नकारात्मक चार्ज इलेक्ट्रॉनों की एक जटिल व्यवस्था है। इस नाभिक में परमाणु का अधिकांश द्रव्यमान होता है और यह प्रोटॉन और न्यूट्रॉन (सामान्य हाइड्रोजन को छोड़कर जो केवल एक प्रोटॉन होता है) से बना होता है।
सभी परमाणु लगभग एक ही आकार के होते हैं। परमाणु आकार मापने के लिए लंबाई की एक सुविधाजनक इकाई एंगस्ट्रॉम (Å) है, जिसे 1 x 10-10 मीटर के रूप में परिभाषित किया गया है। एक परमाणु का व्यास लगभग 2-3 Å है।
1897 में, जे जे थॉमसन ने आधुनिक परमाणु भौतिकी की शुरुआत को चिह्नित करते हुए, इलेक्ट्रॉन के अस्तित्व की खोज की। नकारात्मक चार्ज किए गए इलेक्ट्रॉन नाभिक के चारों ओर परिभाषित ऊर्जा के गोले के भीतर एक यादृच्छिक पैटर्न का पालन करते हैं। परमाणुओं के अधिकांश गुण उनके इलेक्ट्रॉनों की संख्या और व्यवस्था पर आधारित होते हैं। एक इलेक्ट्रॉन का द्रव्यमान 9.1 x 10-31 किलोग्राम है।
नाभिक में पाए जाने वाले दो प्रकार के कणों में से एक प्रोटॉन है। नाभिक में एक सकारात्मक रूप से आवेशित कण, एक प्रोटॉन, का अस्तित्व 1919 में सर अर्नेस्ट रदरफोर्ड द्वारा सिद्ध किया गया था। प्रोटॉन का चार्ज इलेक्ट्रॉन के ऋणात्मक आवेश के बराबर लेकिन बराबर है। एक परमाणु के नाभिक में प्रोटॉन की संख्या यह निर्धारित करती है कि यह किस प्रकार का रासायनिक तत्व है। एक प्रोटॉन का द्रव्यमान 1.67 x 10-27 किलोग्राम होता है।
न्यूट्रॉन नाभिक में पाए जाने वाले अन्य प्रकार के कण हैं। इसकी खोज एक ब्रिटिश भौतिक विज्ञानी सर जेम्स चैडविक ने की थी। न्यूट्रॉन कोई विद्युत आवेश नहीं रखता है और प्रोटॉन के समान द्रव्यमान है। विद्युत आवेश की कमी के साथ, न्यूट्रॉन को इलेक्ट्रॉनों के बादल या नाभिक द्वारा खदेड़ा नहीं जाता है, जिससे यह परमाणु की संरचना की जांच के लिए एक उपयोगी उपकरण बन जाता है।
यहां तक कि व्यक्तिगत प्रोटॉन और न्यूट्रॉन में आंतरिक संरचना होती है, जिसे क्वार्क कहा जाता है। छह प्रकार के क्वार्क मौजूद हैं। इन उप-परमाणु कणों को अलगाव में मुक्त और अध्ययन नहीं किया जा सकता है। वर्तमान अनुसंधान परमाणु की संरचना में जारी है।
परमाणु समस्थानिक (Atomic Isotopes)
परमाणु की एक प्रमुख विशेषता इसकी परमाणु संख्या है, जिसे प्रोटॉन की संख्या के रूप में परिभाषित किया गया है। किसी परमाणु के रासायनिक गुण उसके परमाणु संख्या से निर्धारित होते हैं और इसे प्रतीक Z द्वारा निरूपित किया जाता है। परमाणु में परमाणु (प्रोटॉन और न्यूट्रॉन) की कुल संख्या परमाणु द्रव्यमान संख्या होती है। इस मान को प्रतीक ए द्वारा निरूपित किया जाता है। परमाणु में न्यूट्रॉन की संख्या को एन द्वारा निरूपित किया जाता है। इस प्रकार परमाणु का द्रव्यमान A = N + Z है।
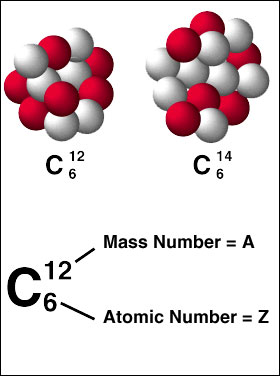

एक ही परमाणु संख्या वाले परमाणु लेकिन अलग-अलग परमाणु द्रव्यमान वाले समस्थानिक कहलाते हैं। आइसोटोप में समान रासायनिक गुण हैं, फिर भी बहुत अलग परमाणु गुण हैं। उदाहरण के लिए, हाइड्रोजन के तीन समस्थानिक हैं। इनमें से दो समस्थानिक स्थिर हैं, (रेडियोधर्मी नहीं), लेकिन ट्रिटियम (एक प्रोटॉन और दो न्यूट्रॉन) अस्थिर हैं। अधिकांश तत्वों में स्थिर समस्थानिक होते हैं। कई तत्वों के लिए रेडियोधर्मी समस्थानिक भी बनाए जा सकते हैं।
आइंस्टीन का समीकरण (Einstein’s Equation)
नाभिक का द्रव्यमान उसके व्यक्तिगत प्रोटॉन और न्यूट्रॉन के द्रव्यमान से लगभग 1 प्रतिशत छोटा है। इस अंतर को द्रव्यमान दोष कहा जाता है। द्रव्यमान दोष उस ऊर्जा से उत्पन्न होता है जब नाभिक (प्रोटॉन और न्यूट्रॉन) नाभिक बनाने के लिए एक साथ बंधते हैं। इस ऊर्जा को बाध्यकारी ऊर्जा कहा जाता है। बाध्यकारी ऊर्जा निर्धारित करती है कि कौन सी नाभिक स्थिर है और एक परमाणु प्रतिक्रिया में कितनी ऊर्जा जारी है। बहुत भारी नाभिक और बहुत हल्के नाभिक में कम बाध्यकारी ऊर्जा होती है। इसका तात्पर्य यह है कि एक भारी नाभिक जब अलग होगा (विखंडन) तो ऊर्जा रिलीज़ करेगा, और जब दो हलके नाभिक जुड़ेंगे (संलयन), तो वे ऊर्जा छोड़ेंगे।
उदाहरण के लिए, हाइड्रोजन 2 नाभिक, एक प्रोटॉन और एक न्यूट्रॉन से बना होता है, इसे ऊर्जा के 2.23 मिलियन इलेक्ट्रॉन वोल्ट (MeV) की आपूर्ति करके पूरी तरह से अलग किया जा सकता है। इसके विपरीत, जब एक धीरे चलने वाला न्यूट्रॉन और प्रोटॉन एक हाइड्रोजन 2 नाभिक बनाने के लिए गठबंधन करते हैं, 2.23 मेव मुक्त होते हैं।
द्रव्यमान दोष और बंधन ऊर्जा अल्बर्ट आइंस्टीन के सूत्र, E = mc2 से संबंधित हैं। 1905 में, आइंस्टीन ने सापेक्षता के विशेष सिद्धांत को विकसित किया। इस सिद्धांत का एक निहितार्थ यह था कि पदार्थ और ऊर्जा एक दूसरे के साथ विनिमेय हैं। यह समीकरण बताता है, एक द्रव्यमान (एम) को ऊर्जा (ई) की मात्रा में परिवर्तित किया जा सकता है, जहां सी प्रकाश की गति है। क्योंकि प्रकाश की गति एक बड़ी संख्या है और इस प्रकार c वर्ग बहुत बड़ा है, पदार्थ की एक छोटी मात्रा को ऊर्जा की जबरदस्त मात्रा में परिवर्तित किया जा सकता है। यह समीकरण परमाणु हथियारों और परमाणु रिएक्टरों की शक्ति की कुंजी है।
रेडियोधर्मी क्षय (Radioactive Decay)
रेडियोधर्मिता परमाणु नाभिक का सहज विघटन है। इस घटना को पहली बार 1896 में फ्रांसीसी भौतिक विज्ञानी हेनरी बेकरेल ने रिपोर्ट किया था। मैरी क्यूरी और उनके पति पियरे क्यूरी ने रेडियोधर्मिता की समझ में और योगदान दिया। उनके शोध ने दो नए रेडियोधर्मी तत्वों, पोलोनियम और रेडियम की खोज की, और वैज्ञानिकों को परमाणु की संरचना के बारे में अपने विचारों को बदलने के लिए मजबूर किया।
रेडियोधर्मिता एक परमाणु का परिणाम है जो एक अधिक स्थिर परमाणु विन्यास तक पहुंचने की कोशिश कर रहा है। रेडियोधर्मी क्षय की प्रक्रिया, तीन प्राथमिक विधियों के माध्यम से प्राप्त की जा सकती है; एक नाभिक अपने न्यूट्रॉन को प्रोटॉन में बदलकर एक इलेक्ट्रॉन (बीटा क्षय) के एक साथ उत्सर्जन कर सकता है, एक हीलियम नाभिक (अल्फा क्षय), या दो टुकड़ों में सहज विखंडन (विभाजन) द्वारा। अक्सर इन घटनाओं से जुड़े उच्च ऊर्जा फोटॉन या गामा किरणों की रिहाई होती है। रेडियोधर्मी क्षय के कुछ अन्य तरीके हैं, लेकिन वे प्रकृति में अधिक विदेशी हैं।
प्रत्येक व्यक्तिगत रेडियोधर्मी पदार्थ की एक विशेषता क्षय अवधि या आधा जीवन है। एक अर्ध-जीवन एक रेडियोधर्मी नमूने के परमाणु नाभिक के आधे से क्षय के लिए आवश्यक समय का अंतराल है। रेडियोएक्टिव आइसोटोप कोबाल्ट 60, जिसका उपयोग विकिरण कैंसर चिकित्सा में किया जाता है, उदाहरण के लिए, 5.26 वर्षों का आधा जीवन। इस प्रकार उस अंतराल के बाद, एक नमूना जिसमें मूल रूप से 16 ग्राम कोबाल्ट 60 होता है, उसमें केवल 8 ग्राम कोबाल्ट 60 होता है और यह केवल आधे से अधिक विकिरण का उत्सर्जन करेगा। 5.26 वर्षों के एक और अंतराल के बाद, नमूना में केवल 4 ग्राम कोबाल्ट 60 होगा। आधा जीवन हजारों साल से लेकर मिलीसेकंड तक हो सकता है।
कभी-कभी रेडियोधर्मी क्षय से गुजरने के बाद, नए परमाणु को अभी भी एक रेडियोधर्मी रूप में छोड़ दिया जाता है। इसका मतलब यह है कि परमाणु फिर से क्षय होगा क्योंकि यह एक स्थिर परमाणु स्थिति तक पहुंचने का प्रयास करता है।
अल्फा क्षय (Alpha Decay)
अल्फा क्षय में, एक सकारात्मक चार्ज कण, हीलियम 4 के नाभिक के समान, अनायास उत्सर्जित होता है। इस कण को अल्फा कण के रूप में भी जाना जाता है, इसमें दो प्रोटॉन और दो न्यूट्रॉन होते हैं। इसे 1899 में सर अर्नेस्ट रदरफोर्ड द्वारा खोजा और नाम दिया गया था।


अल्फा क्षय आमतौर पर यूरेनियम या प्लूटोनियम जैसे भारी नाभिक में होता है, और इसलिए यह परमाणु विस्फोट से रेडियोधर्मी गिरावट का एक प्रमुख हिस्सा है। चूंकि एक अल्फा कण रेडियोधर्मी क्षय के अन्य रूपों की तुलना में अपेक्षाकृत अधिक विशाल है, इसे कागज की एक शीट द्वारा रोका जा सकता है और मानव त्वचा में प्रवेश नहीं कर सकता है। एक 4 MeV अल्फा कण केवल 1 इंच हवा के माध्यम से यात्रा कर सकता है।
हालांकि एक अल्फा कण की सीमा कम है, अगर एक अल्फा क्षय तत्व को निगला जाता है, तो अल्फा कण आसपास के ऊतक को काफी नुकसान पहुंचा सकता है। यही कारण है कि लंबे जीवन के साथ प्लूटोनियम, अगर निगला जाता है तो बेहद खतरनाक है।
बीटा क्षय (Beta Decay)
एटम बीटा कणों को एक प्रक्रिया के माध्यम से उत्सर्जित करते हैं जिन्हें बीटा क्षय के रूप में जाना जाता है। बीटा क्षय तब होता है जब एक परमाणु में बहुत अधिक प्रोटॉन या बहुत से न्यूट्रॉन होते हैं। दो प्रकार के बीटा क्षय हो सकते हैं। एक प्रकार (सकारात्मक बीटा क्षय) पॉज़िट्रॉन नामक एक सकारात्मक रूप से चार्ज बीटा कण और एक न्यूट्रिनो को जारी करता है; अन्य प्रकार (ऋणात्मक बीटा क्षय) एक नकारात्मक रूप से आवेशित बीटा कण को जारी करता है जिसे इलेक्ट्रॉन, और एक एंटीन्यूट्रिनो कहा जाता है। न्यूट्रिनो और एंटीन्यूट्रिनो बहुत कम या कोई द्रव्यमान वाला उच्च ऊर्जा प्राथमिक कण होते हैं और क्षय प्रक्रिया के दौरान ऊर्जा के संरक्षण के लिए जारी किए जाते हैं। नकारात्मक बीटा क्षय सकारात्मक बीटा क्षय की तुलना में कहीं अधिक सामान्य है।
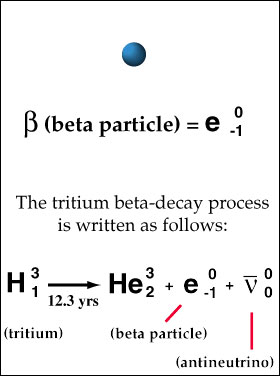

रेडियोएक्टिव क्षय के इस रूप की खोज 1899 में सर अर्नेस्ट रदरफोर्ड ने की थी, हालाँकि 1960 तक न्यूट्रिनो का अवलोकन नहीं किया गया था। बीटा कणों में इलेक्ट्रॉनों की सभी विशेषताएं होती हैं। अपने उत्सर्जन के समय, वे लगभग प्रकाश की गति से यात्रा करते हैं। एक विशिष्ट .5 मेव कण हवा के माध्यम से लगभग 10 फीट की यात्रा करेगा, और इसे 1-2 इंच की लकड़ी से रोका जा सकता है।
गामा किरणें (Gamma Rays)
गामा किरणें विद्युत चुम्बकीय विकिरण का एक प्रकार हैं जो एक नाभिक के भीतर विद्युत आवेश के पुनर्वितरण से उत्पन्न होती हैं। गामा किरणें अनिवार्य रूप से बहुत ऊर्जावान एक्स किरणें हैं; दोनों के बीच अंतर उनके आंतरिक स्वभाव पर आधारित नहीं है, बल्कि उनके मूल पर है। ऊर्जावान इलेक्ट्रॉनों को शामिल करने वाली परमाणु प्रक्रियाओं के दौरान एक्स किरणों का उत्सर्जन होता है। गामा विकिरण उत्सर्जित नाभिक या अन्य प्रक्रियाओं से उत्सर्जित होता है जिसमें उप-परमाणु कण शामिल होते हैं; यह अक्सर अल्फा या बीटा विकिरण के साथ होता है, क्योंकि उन कणों को उत्सर्जित करने वाले एक नाभिक को एक उत्तेजित (उच्च-ऊर्जा) स्थिति में छोड़ा जा सकता है।
गामा किरणें अल्फा या बीटा विकिरण की तुलना में अधिक मर्मज्ञ हैं, लेकिन कम आयनीकरण। परमाणु पतन से गामा किरणें संभवतः परमाणु युद्ध में परमाणु हथियारों के उपयोग की घटना में सबसे बड़ी संख्या में हताहतों की संख्या का कारण बनेंगी। वे एक्स-रे जैसे जलने, कैंसर, और आनुवंशिक उत्परिवर्तन के कारण होने वाली क्षति के समान हैं।
सहज विखंडन (Spontaneous Fission)
एक अन्य प्रकार का रेडियोधर्मी क्षय सहज विखंडन है। इस क्षय प्रक्रिया में, नाभिक लगभग दो समान टुकड़ों और कई मुक्त न्यूट्रॉन में विभाजित होगा। बड़ी मात्रा में ऊर्जा भी जारी की जाती है। अधिकांश तत्व इस तरह से क्षय नहीं करते हैं जब तक कि उनकी द्रव्यमान संख्या 230 से अधिक न हो।
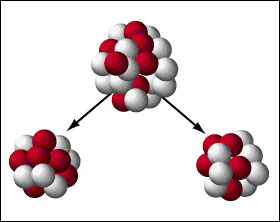

एक सहज विखंडन द्वारा जारी आवारा न्यूट्रॉन समय से पहले एक श्रृंखला प्रतिक्रिया शुरू कर सकते हैं। इसका मतलब यह है कि एक महत्वपूर्ण द्रव्यमान तक पहुंचने के लिए विधानसभा का समय सहज विखंडन की दर से कम होना चाहिए। वैज्ञानिकों को परमाणु हथियारों को डिजाइन करते समय प्रत्येक सामग्री की सहज विखंडन दर पर विचार करना होगा।
उदाहरण के लिए, प्लूटोनियम 239 की सहज विखंडन दर यूरेनियम 235 की तुलना में लगभग 300 गुना अधिक है। यह मैनहट्टन प्रोजेक्ट पर काम करने वाले वैज्ञानिकों को एक बंदूक-प्रकार के डिजाइन पर काम छोड़ने के लिए मजबूर करता है जो प्लूटोनियम का उपयोग करता था।
[ratemypost]
इस लेख से सम्बंधित अपने सवाल और सुझाव आप नीचे कमेंट में लिख सकते हैं।


परमाणु पर टिप्पणी