विषय-सूचि
कार्बन (Carbon)
कार्बन पीरियोडिक टेबल पर नंबर 6 पर रखा गया है और यह ब्रह्मांड में और पृथ्वी की परत में सबसे प्रचुर मात्रा में व्याप्त तत्वों में से एक है। इसे सभी जीवों का मौलिक बिल्डिंग ब्लॉक भी माना जाता है। इसलिए, कार्बन के कंपाउंड्स को आर्गेनिक कंपाउंड्स के रूप में जाना जाता है, और कार्बन कंपाउंड्स के अध्ययन को आर्गेनिक रसायन शास्त्र के रूप में जाना जाता है।
कार्बन फ्री स्टेट के साथ-साथ कंबाइंड स्टेट में कई अन्य तत्वों के साथ प्रकृति में होता है। वास्तव में, हाइड्रोजन के बाद, यह तत्व ही ऐसा है जो अन्य तत्वों के साथ कंपाउंड्स की सबसे अधिक संख्या बनाता है। कार्बन चक्र के जरिये आप इसे समझ सकते हैं।
कार्बन प्रमुख अणुओं का एक प्रमुख टुकड़ा है जो पृथ्वी पर सभी जीवित चीजें बनाते हैं। यह ग्लूकोज, प्रोटीन, फैट, सेलूलोज़ और डीएनए का एक महत्वपूर्ण हिस्सा है। इसके अतिरिक्त, कार्बन चूना पत्थर और एस्फाल्ट, जीवाश्म ईंधन जैसे प्राकृतिक गैस और पेट्रोलियम, लकड़ी, प्लास्टिक और कई अन्य पदार्थों जैसे चट्टानों का एक प्रमुख घटक भी है। कार्बन डेटिंग चीजों की अनुमानित आयु दे देता है।
कार्बन को विभिन्न रूपों में प्रकृति में फ्री स्टेट में पाया जाता है, जिसे कार्बन के आवंटन या ऐलोट्रोप(allotropes) के रूप में जाना जाता है।
एलोट्रोपि क्या है? (allotropy in hindi)
एलोट्रोपि कुछ रासायनिक तत्वों की प्रॉपर्टी है जो प्रकृति में फ्री में पाए जाने पर दो या दो से अधिक विभिन्न भौतिक रूपों में मौजूद हैं। तत्व के विभिन्न रूपों को एलोट्रॉप के रूप में जाना जाता है। ये एलोट्रोप विभिन्न भौतिक गुणों को प्रदर्शित करते हैं लेकिन समान श्रेणीबद्ध रासायनिक गुण प्रदर्शित करते हैं। एलोट्रॉपी तत्व के परमाणुओं की संरचनात्मक व्यवस्था में अंतर का परिणाम है।
कार्बन उन तत्वों में से एक है जो एलोट्रॉपी प्रदर्शित करते हैं। क्रिस्टलीय रूप के साथ-साथ असंगत रूप में कार्बन के कई आलोट्रोप भी हैं।
कार्बन के एलोट्रॉप (carbon allotropes in hindi)
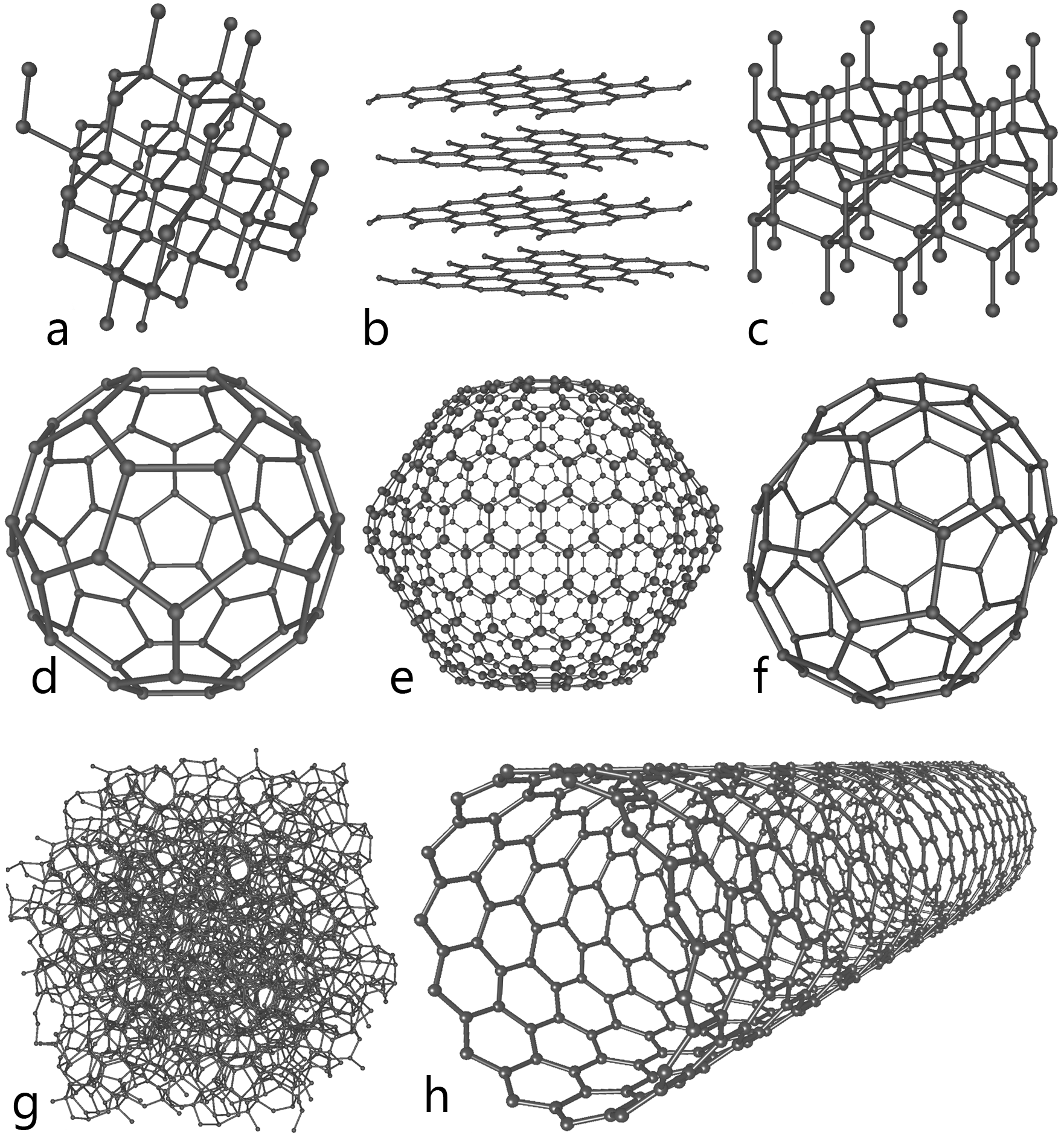
कार्बन में दो क्रिस्टलीय आवंटन होते हैं- हीरा और ग्रेफाइट। रसायनविदों ने प्रयोगशाला में कार्बन के तीसरे, नए क्रिस्टलीय एलोट्रोप का निर्माण किया और इसे फुलेरिन नाम दिया।
हीरा (Diamond)
हीरा एक पारदर्शी, चमकदार और अत्यंत कठिन, कार्बन का क्रिस्टलीय रूप है।
मनुष्य द्वारा जाना गया डायमंड सबसे कठिन पदार्थ माना जाता है। प्रत्येक कार्बन एटम टेट्राहेड्रल रूप में चार अन्य कार्बन एटम से जुड़ा होता है। यह डायमंड की क्रिस्टलीय संरचना बनाता है। यह मूल इकाई खुद को दोहराती है और एक ऑक्टाहेड्रल जाली बनाने के लिए सभी दिशाओं में फैल जाती है। इसके अतिरिक्त, एटम्स के बीच का बांड या बंधन बहुत मजबूत कोवेलेन्ट बांड(covalent bond) होते हैं।
डायमंड के उपयोग (uses of diamond in hindi)
इसकी कठोरता के कारण, उद्योग में काटने, ड्रिलिंग और पीसने के उद्देश्यों के लिए हीरे का उपयोग किया जाता है। इन्हें सेमी-कंडक्टर बनाने में उपयोग किया जाता है। इनका सबसे महंगे आभूषणों में कीमती रत्नों के रूप में भी उपयोग किया जाता है।
ग्रेफाइट (Graphite in hindi)
ग्रेफाइट कार्बन का एक भूरा काला, चमकदार और मुलायम क्रिस्टलीय रूप है।
ग्रेफाइट की संरचना एक द्वि-आयामी हेक्सागोनल इकाई से बनाई गई है, जिसमें प्रत्येक कार्बन एटम एक ही परत में कोवेलेन्ट बांड(covalent bond) द्वारा तीन अन्य कार्बन एटम्स से जुड़ा होता है, इस प्रकार यह इसे एक शीट जैसी संरचना प्रदान करता है। परतों को एक दूसरे के ऊपर समानांतर में व्यवस्थित किया जाता है, जो कमजोर वान डेर वाल्स बलों(Van der Waals forces) द्वारा एक साथ आयोजित किया जाता है। यही कारण है कि ग्रेफाइट एक नरम, स्लीपरी सॉलिड है, जो कागज पर एक काला निशान छोड़ देता है। इसके अतिरिक्त, क्रिस्टल में इसकी संरचना में मोबाइल इलेक्ट्रॉन हैं, इस प्रकार यह गर्मी और बिजली का एक अच्छा कंडक्टर बन जाता हैं, भले ही यह एक नॉन-मेटल क्यों न है।
ग्रेफाइट का उपयोग (graphite uses in hindi)
इसकी मुलायम प्रकृति के कारण, और पेपर ब्लैक को चिह्नित करने की क्षमता के कारण, ग्रेफाइट का उपयोग पेंसिल लीड बनाने और मशीन के गर्म भागों, सामान्य मशीन भागों और साइकिल श्रृंखलाओं के लिए लुब्रीकेंट के रूप में किया जाता है। चूंकि यह बिजली का एक अच्छा, स्थिर कंडक्टर है, इसलिए इसे ड्राई सेल, इलेक्ट्रोलाइटिक कोशिकाओं और इलेक्ट्रोप्लाटिंग में इलेक्ट्रोड के रूप में और अपवर्तक क्यूबिकल्स के निर्माण में उपयोग किया जाता है।
फुलरीन (fullerene in hindi)
Fullerenes पिंजरे की तरह के मॉलिक्यूल्स जैसे हैं। C60 मॉलिक्यूल में सॉकर बॉल की तरह एक आकार होता है और जिसे बकमिंस्टर फुलेरिन कहा जाता है।
सभी कार्बन एटम बराबर हैं और वे sp2 हाइब्रिडाइजेशन से गुजरते हैं।
ग्रेफाइट थर्मोडायनामिक रूप से सबसे स्थिर माना गया है।
कार्बन का उपयोग किसमें किया जाता है:
- प्लास्टिक सामग्री में एम्बेडेड ग्रेफाइट फाइबर उच्च शक्ति और हल्के कंपोजिट्स बनाते हैं।
- कंपोजिट्स का उपयोग टेनिस रैकेट, मछली पकड़ने की छड़, एयरक्राफ्ट और डिब्बे जैसे उत्पादों में किया जाता है।
- अच्छे कंडक्टर होने के नाते, बैटरी और औद्योगिक इलेक्ट्रोलिसिस में इलेक्ट्रोड के लिए ग्रेफाइट का उपयोग किया जाता है।
- सक्रिय लकड़ी का कोयला: जहरीले गैसों की adsorbing; आर्गेनिक दूषित पदार्थों को हटाने और गंध को नियंत्रित करने के लिए एयरकंडीशनिंग सिस्टम के जल फ़िल्टर में भी प्रयोग किया जाता है।
- कार्बन ब्लैक: ब्लैक स्याही में ब्लैक पिग्मेंट और ऑटोमोबाइल टायर में फिलर के रूप में।
- कोक: एक ईंधन और धातु विज्ञान में एक घटते एजेंट के रूप में।
- डायमंड एक कीमती पत्थर है और आभूषणों में प्रयोग किया जाता है। यह कैरेट में मापा जाता है (1 कैरेट = 200 मिलीग्राम)।
इस लेख से सम्बंधित यदि आपका कोई भी सवाल या सुझाव है, तो आप उसे नीचे कमेंट में लिख सकते हैं।