विषय-सूचि
आदर्श गैस क्या है? (ideal gas meaning in hindi)
आदर्श गैस (ideal gas) को हम एक सैद्धांतिक गैस के रूप में देखते है जो कई random रूप से चलते छोटे छोटे पार्टिकल या पॉइंट पार्टिकल्स से बना है, जिनकी इंटरैक्शन पूरी तरह से इलास्टिक collision हैं।
नाइट्रोजन, ऑक्सीजन, हाइड्रोजन, नोबल गैसो जैसी कई गैसें और कार्बन डाइऑक्साइड जैसी कुछ भारी गैसों को उचित सहनशीलता के भीतर आदर्श गैसों की तरह माना जा सकता है।
आदर्श गैस और वास्तविक गैस में अंतर (difference in real and ideal gas in hindi)
कोई भी पदार्थ तरल, ठोस, और गैस के रूप में होता है। जिन्हें उनकी मुख्य विशेषताओं के माध्यम से पहचाना जाता है।
ठोस पदार्थों में मॉलिक्यूल्स की संरचना मजबूत होती है जो उन्हें निश्चित आकार और द्रव्यमान प्रदान करती है, तरल पदार्थ उनके कंटेनर का रूप लेते हैं क्योंकि मॉलिक्यूल एक दूसरे के अनुरूप होते हैं, और गैसों को हवा में फैलती है क्योंकि मॉलिक्यूल स्वतंत्र रूप से आगे बढ़ रहे हैं।
गैसों की विशेषताएं बहुत अलग हैं। ऐसी गैसे हैं जो अन्य पदार्थों के साथ प्रतिक्रिया करने के लिए पर्याप्त मजबूत हैं, यहां तक कि बहुत मजबूत गंध के साथ भी हैं, और कुछ पानी के साथ भी मिल सकती हैं। असली गैसों का व्यवहार बहुत जटिल होता है जबकि आइडियल गैसों का व्यवहार बहुत आसान होता है।
इस आदर्श गैस को “पॉइंट मास” के रूप में माना जा सकता है। इसका मतलब यह है कि पार्टिकल बहुत छोटा है और इसका द्रव्यमान लगभग शून्य है। आइडियल गैस पार्टिकल में मात्रा नहीं है, जबकि वास्तविक गैस पार्टिकल में वास्तविक मात्रा होती है क्योंकि वास्तविक गैस मॉलिक्यूल्स या एटम्स से बने होते हैं जो आमतौर पर कुछ जगह लेते हैं, भले ही वे बहुत छोटे हो।
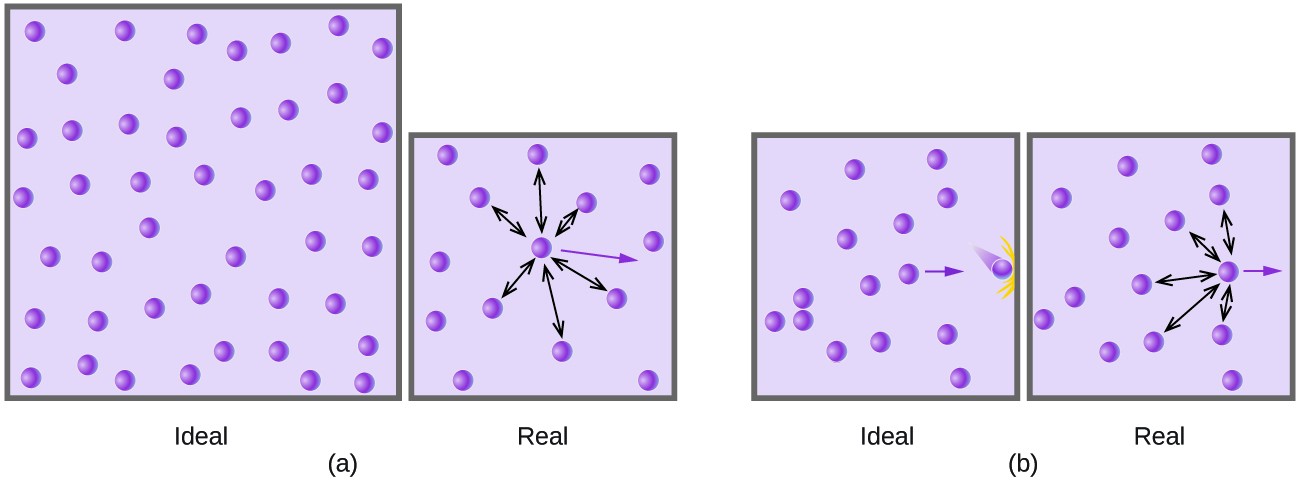
आदर्श गैस में, पार्टिकल के बीच टकराव या प्रभाव को elastic कहा जाता है। इसके विपरीत, असली गैसों में पार्टिकल के टकराव को non-elastic कहा जाता है। वास्तविक गैस पार्टिकल्स या मॉलिक्यूल्स से बने होते हैं जो पानी वाष्प, अमोनिया, सल्फर डाइऑक्साइड आदि जैसे प्रतिकूल ऊर्जा या आकर्षक बल के व्यय के साथ एक दूसरे को बहुत दृढ़ता से आकर्षित कर सकते हैं।
असली गैस के प्रेशर की तुलना में आइडियल गैस में प्रेशर बहुत अधिक होता है क्योंकि पार्टिकल्स के बीच आकर्षक ताकत नहीं होती है जो अणुओं को एक प्रभाव पर टकराने के बाद वापस पकड़ने में सक्षम हो। इसलिए, पार्टिकल कम ऊर्जा के साथ टकराते हैं।
आदर्श गैस के गुण (properties of ideal gas in hindi)
एक आइडियल गैस के मुख्य गुण होते हैं:
- एक आइडियल गैस के मॉलिक्यूल्स के बीच कोई इंटरेक्शन नहीं होता;
- एक आइडियल गैस के मॉलिक्यूल्स में कोई मात्रा नहीं होती;
- सभी गैसों के रूप में, आइडियल गैस का आकार नहीं होता है, इसलिए इसमें किसी भी प्रकार के कंटेनर को भरने की संपत्ति होती है;
आदर्श गैस का समीकरण (ideal gas law formula in hindi)
आदर्श गैस का नियम फार्मूला प्रेशर, मात्रा और तापमान से संबंधित है:
P*V = n*R*T
P- प्रेशर; V- मात्रा या वॉल्यूम; N- गैस के मोल; R- गैस कांस्टेंट; T- तापमान जो केल्विन इकाइयों में व्यक्त किया जाना चाहिए।
आदर्श गैस और काइनेटिक सिद्धांत (ideal gas and kinetic rule in hindi)
आइडियल गैस जैसी कोई चीज नहीं है, लेकिन कई गैसों का व्यवहार लगभग वैसा ही लगता है जैसे कि वे साधारण तापमान और दबाव में आइडियल थी।
आइडियल गैसों के बारे में धारणाएं है कि:
- ये गैस मॉलिक्यूल्स से बनी होती हैं जो सीधे लाइनों में निरंतर यादृच्छिक(random) गति में होती हैं।
- दबाव यानी प्रेशर मॉलिक्यूल्स और कंटेनर की दीवारों के बीच टकराव के कारण होता है।
- सभी टकराव, मॉलिक्यूल्स के बीच, और मॉलिक्यूल्स और कंटेनर की दीवारों के बीच, पूरी तरह से elastic हैं। (इसका मतलब है कि टकराव के दौरान काइनेटिक ऊर्जा का कोई नुकसान नहीं होता है।)
- गैस का तापमान मॉलिक्यूल्स की औसत काइनेटिक ऊर्जा के समान होता है।
आदर्श गैस का नियम (ideal gas equation in hindi)
pV= nRT
विभिन्न टर्म्स:
- प्रेशर, P
प्रेशर पास्कल(pascal) में मापा जाता है, Pa कभी-कभी प्रति वर्ग मीटर में भी मापा जाता है, Nm^-2 ।
कभी कभी आपको kPa (किलोपास्कल्स) में भी प्रेशर दिया जाता है। उदाहरण के लिए, 150 kPa ही 150000 Pa है। आइडियल गैस equation का उपयोग करने से पहले आपको यह रूपांतरण करना होगा। - वॉल्यूम, V
जब आप इस equation का उपयोग करते हैं तो यह सबसे संभावित स्थान जहां हम गलती कर सकते हैं । ऐसा इसलिए है क्योंकि वॉल्यूम की एसआई यूनिट cubic metre, m^3 है – cm^3 या dm^3 नहीं है।
1 m^3 = 1000 dm^3 = 1000000 cm^3
तो यदि आप equation में वॉल्यूम का मान डाल रहे हैं, तो आपको पहले उसे क्यूबिक मीटर में परिवर्तित करना होगा।मॉल्स(moles) की संख्या, N
ज़ाहिर है – यह सिर्फ एक संख्या है।
- गैस कांस्टेंट, R
आर के लिए एसआई यूनिट 8.31441 J K^-1 mol^-1 है। - तापमान, T
तापमान केल्विन में होना चाहिए। यदि आपको डिग्री सेल्सियस में तापमान दिया जाता है तो 273 जोड़कर आप उसे केल्विन में बदल सकते हैं।
इस लेख के बारे में यदि आपका कोई भी सवाल या विचार है, तो आप उसे नीचे कमेंट में लिख सकते हैं।

aadarsh gas simple gases se kis taraah alag hai and kyaa iski koi particular smell bhi hoti hai??
ake quschen ko example leke karo
Bahut achhe se smjh me aya