विषय-सूचि
डाल्टन के परमाणु सिद्धांत की परिभाषा (dalton’s atmoic theory definition in hindi)
डाल्टन के परमाणु सिद्धांत के अनुसार, “प्रत्येक पदार्थ छोटे-छोटे कणों से मिलकर बना होता है जिन्हें परमाणु कहते हैं और परमाणु को किसी भी भौतिक या रासायनिक विधि से विभाजित नहीं किया जा सकता है।”
पदार्थ (matter) हमेशा से ही वैज्ञानिकों के बीच शोध का अति महत्वपूर्ण विषय रहा है। वैज्ञानिक हमेशा से जानना चाहते थे कि पदार्थ किन मूलभूत कणों से मिलकर बना है। उनके गुण क्या होते हैं। उनका आकार कैसा है।
यही कारण था इस विषय को लेकर अनेक सिद्धांत प्रतिपादित हुए। इन सवालो के हल जानने का पहला प्रयास एक ब्रिटिश अध्यापक जॉन डाल्टन ने सन् 1808 में किया। डाल्टन का परमाणु सिद्धांत द्रव्यमान संरक्षण का नियम (law of mass conservation) और स्थिर अनुपात का नियम (Law of constant proportion) पर आधारित था।
डाल्टन के सिद्धांत के मुख्य बिंदु (main points of dalton’s atmoic theory in hindi)
इस सिद्धांत के प्रमुख बिंदु निम्न हैं-
- प्रत्येक तत्व अतिसूक्ष्म अविभाज्य कणों से मिलकर बना है जिन्हें परमाणु (atom)कहते हैं।
- एक तत्व की सभी परमाणु आकार तथा गुणों में समान होते हैं किंतु भिन्न-भिन्न तत्वों के परमाणु भिन्न-भिन्न होते हैं।
- भिन्न भिन्न तत्वों के परमाणु के गुण भी भिन्न भिन्न होते हैं।
- परमाणु अविनाशी (indestructible) होता है अर्थात रासायनिक अभिक्रिया में परमाणु ना तो उत्पन्न होते हैं और ना ही नष्ट होते हैं।
- तत्वों के परमाणु वापस में संयोग करके संयुक्त परमाणु बनाते हैं तथा आधुनिक शब्दों में इस संयुक्त परमाणु को अणु कहते हैं।
- बनने वाले संयुक्त परमाणु में परमाणुओं कि आपेक्षिक संख्या और उनका प्रकार निश्चित होता है।
डाल्टन परमाणु सिद्धांत के अनुप्रयोग (applications of dalton’s atomic theory in hindi)
- डाल्टन के परमाणु सिद्धांत पदार्थ की संरचना के मूलभूत विचार को प्रस्तुत करता है। इसके अनुसार परमाणु पदार्थ के निर्माण की सबसे छोटी इकाई है।
- डाल्टन का परमाणु सिद्धांत उस समय तक ज्ञात रासायनिक संयोग के नियम (Law of chemical composition) की अवधारणा को समाहित करता है,जैसे बिंदु (4) द्रव्यमान संरक्षण तथा बिंदु (5) निश्चित अनुपात के नियम को प्रदर्शित करता है।
- डाल्टन का परमाणु सिद्धांत गुणित अनुपात के नियम (Law of multiple proportion) की भी व्याख्या करता है।
- यह सिद्धांत भिन्न भिन्न तत्वों के परमाणुओं में विभिन्नता को भी प्रदर्शित करता है।
डाल्टन परमाणु सिद्धांत की सीमाएं (limitations of dalton’s atomic theory in hindi)
- डाल्टन के अनुसार तत्वों के निर्माण की सूक्ष्मतम इकाई परमाणु है जबकि यौगिक की सूक्ष्मतम इकाई संयुक्त परमाणु (compound atom) है, वास्तव में जिस संयुक्त परमाणु की अवधारणा डाल्टन ने प्रस्तुत की वह अणु था।
- यह सिद्धांत बर्जीलियस परिकल्पना की व्याख्या नहीं करता जिसने प्रतिपादित किया कि ताप व दाब की समान परिस्थितियों में गैसों के समान आयतन में परमाणुओं की संख्या समान होती है।
- यह सिद्धांत इस तथ्य की व्याख्या नहीं करता कि परमाणु आपस में क्रिया करके अणु क्यों बनाते हैं।
- यह परमाणुओं तथा अणुओं की ठोस, द्रव एवं गैस की भौतिक अवस्थाओं में बलों की प्रकृति के विषय में कोई प्रकाश नहीं डालता है।
- यह समस्थानिकों (isotopes) की उपस्थिति तथा गेलुसाक के आयतन नियम (law of gaseous volumes) की व्याख्या नहीं करता है।
- यह सिद्धांत इस तथ्य की भी व्याख्या नहीं करता है कि भिन्न भिन्न तत्वों के परमाणु का द्रव्यमान, आकार और संयोजकता (valency) अलग-अलग क्यों होती है।
डाल्टन परमाणु सिद्धांत की वर्तमान स्थिति (current position of dalton’s atmoic theory in hindi)
- इलेक्ट्रॉन, प्रोटॉन ,न्यूट्रॉन तथा अन्य उप परमाण्विक (sub-atomic) कणों की खोज से यह सिद्ध हो चुका है कि परमाणु अविभाज्य नहीं है।
- समस्थानिकों (isotopes)की खोज के पश्चात यह सिद्ध हो चुका है कि एक ही तत्व के परमाणुओं के परमाणु द्रव्यमान भिन्न भिन्न हो सकते हैं।
- समभारिक (isobars) की खोज के बाद यह सिद्ध हो चुका है कि भिन्न भिन्न तत्वों के परमाणु के द्रव्यमान समान हो सकते हैं।
- नाभिकीय रसायन के उदय के पश्चात एक परमाणु का दूसरे परमाणु में परिवर्तन संभव हो गया है।
- परमाणु आपस में भिन्नात्मक अनुपात में भी क्रिया कर सकते हैं।
आधुनिक परमाणुवाद भले ही डाल्टन के परमाणु सिद्धांत से अलग है लेकिन रसायन विज्ञान में उनके योगदान का बहुत ही महत्व है क्योंकि उनके सिद्धांत देने के बाद ही इलेक्ट्रॉन, प्रोटॉन न्यूट्रॉन तथा अन्य कणों की खोज हुई।
कई अवधारणा के बारे में दुनिया को पता चला और इन सब कारणों से डाल्टन का परमाणु सिद्धांत रसायन विज्ञान का सैद्धांतिक आधार बना।
इस विषय से सम्बंधित यदि आपका कोई सवाल या सुझाव है, तो आप उसे नीचे कमेंट के जरिये हमसे पूछ सकते हैं।

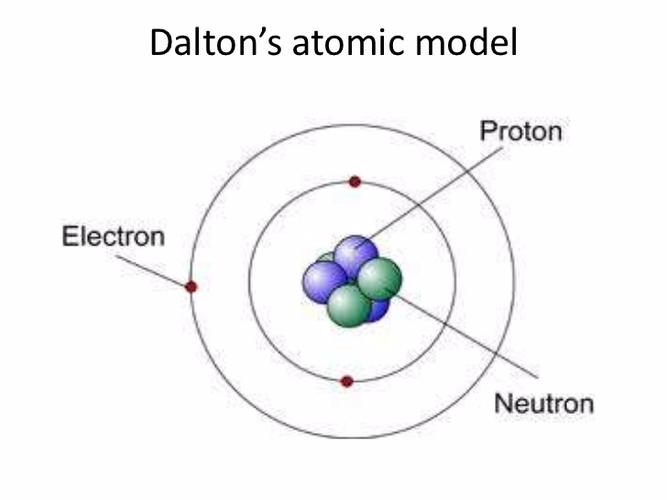
dalton aur bohr ke atomic model structure mein kya differnce hai? bohr ka model bahut easy hai samjhne mein.
डाल्टन का परमाणु सिद्धांत अणु की संरचना को बहुत सरल तरीके से समझाता है.
Maine Dalton ke. Baare me apni science class me padha lekin apka post padhne ke baad jyada acche se samajh me aaya
I wanna thank you
डाल्टन का सिद्धांत फेल क्यों हो गया था सर? और इसमें क्या कमियां थी?
dalton ke parmanu siddhant mein aisi kyaa kamiyaan reh gayi thi ki vah chala nahi? vah fail kyon ho gayaa thaa?
Dalton ne apne parmanu siddhant mein isotopes ke baare mein Kya jaankaari di hai? Kya yah jaankaari sahi hai?
Nahi Dalton ne apne parmanu Siddhant mein isotopes ki jankari nahin Di hai usne kaha hai ki parmanu Siddhant ke anusar ek hi tatv ke sabhi parmanu Sharma saman dravyaman wale hote Hain Jo ki Sahi nahin hai tatv ke parmanu vibhinn dravyaman Wale bhi hote Hain jinhen isotopes khate Hain
Yes
NICE IT IS EASY TO UNDERSTAND
THANKS;
Very easy to understand sir
Thanku so much
Due to this I understand Dalton’s atomic theory.
Thank you sir
Thank you I am understand dalton theory
Thank you sir
I am totally understand dallton theory
##thanks a lot sir###
Thanks Sir
Thanku sir
Thank you sir
Thnx sir